無常規靶藥可用,免疫藥物獲益低,化療是否是最后的方案?2019-07-18 09:56
 小編,我想請問一下,基因檢測報告陰性顯示無常規對應靶向藥物,又做了PD-L1表達、TMB、MSI檢測,拿到報告還是均為陰性,除了化療是否還有更佳的方案? 這種情況確實比較棘手,即無常規對應靶向藥物,免疫檢查點 抑制劑藥物又獲益不佳且價格昂貴。但其實除了化療藥物治療,其實還有一類藥物—腫瘤血管生成抑制劑可以選擇。 接下來就讓小編好好給你介紹一下吧~  小編 在介紹腫瘤血管生成抑制劑之前,小編先來給各位介紹一下腫瘤的血管生成。血管生成是腫瘤發展惡化的基礎,維持腫瘤細胞生長的基礎是充足的營養物質,而運輸營養物質的媒介即是腫瘤血管。 在腫瘤細胞發生早期,腫瘤細胞可以通過組織滲透維持生長。但當其直徑超過2mm之后,必須構建提供自身營養的血管系統。腫瘤細胞通過分泌血管生成調節因子,來促進腫瘤自身血管的生成,為其提供生長和發展必須的營養和氧氣,并在腫瘤細胞浸潤、生長和轉移中起到關鍵作用。
腫瘤血管相關調節因素可以分為:
上述兩種機制構成了靶向腫瘤血管生成藥物的靶點基礎,臨床應用的抗血管生成藥物主要有以下三類:
國內批準上市的腫瘤血管生長抑制劑
由于腫瘤血管生成抑制劑獲批癌種適應癥較多,小編無法在這里一一介紹,今天小編將選擇獲批非小細胞肺癌適應癥的三款藥物:貝伐珠單抗、安羅替尼、重組人血管內皮抑制劑,來介紹其在非小細胞肺癌領域的相關獲批信息及臨床試驗數據。 貝伐珠單抗(Bevacizumab, Avastin, 安維汀)一種人源化IgG1,通過與人血管內皮生長因子(VEGF)結合并阻斷其生物活性從而抑制腫瘤組織內產生新的血管。2004年2月26日,成為FDA批準的第一個抑制腫瘤血管生成的藥。2010年2月獲得中國原CFDA批準上市。 2018年10月獲批新適應癥:貝伐珠單抗聯合以鉑類為基礎的化療用于不可切除的晚期、轉移性或復發性非鱗狀細胞非小細胞肺癌患者的一線治療。
2006年一項三期隨機多中心隨機試驗,旨在研究復發、晚期或轉移非鱗狀NSCLC患者接受貝伐單抗+紫杉醇和卡鉑對比紫杉醇和卡鉑的差異。 結果顯示:相比較對照組,貝伐單抗組的中位生存期從10.3個月延長到12.3個月,增長了2個月(HR=0.80,P=0.013),同時基于未獨立驗證的研究者評估,貝伐單抗組擁有更長的PFS。 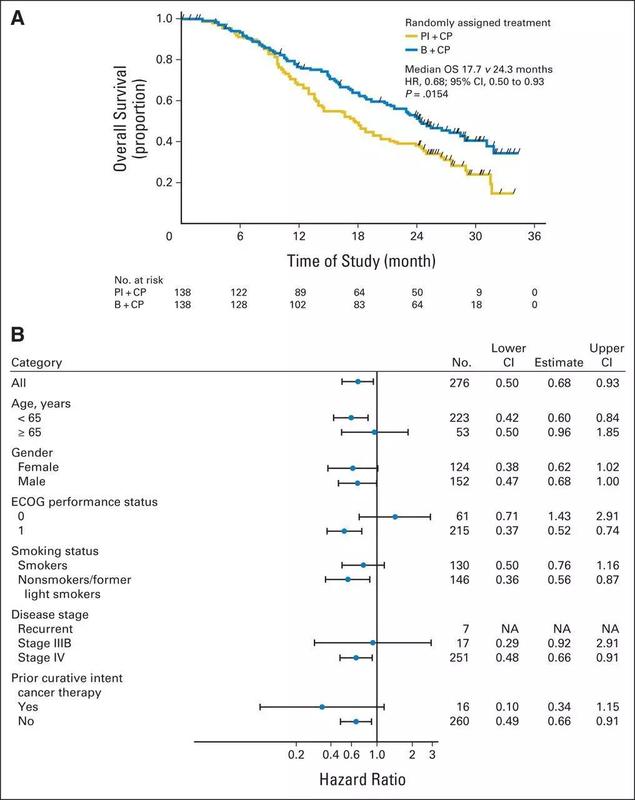 我國開展的BEYOND隨機雙盲臨床研究中,276例晚期非鱗非小細胞肺癌患者隨機分為貝伐珠單抗組和安慰劑組,所有患者均接受紫杉醇加卡鉑的聯合化療。 結果顯示:貝伐珠單抗組與安慰劑組的ORR分別為54%和26%(P<0.001),中位PFS分別為9.2和6.5個月(HR 0.40,P<0.001),中位OS分別為24.3個月和17.7個月(HR 0.68,P=0.0154),疾病無進展風險和生存風險分別降低了60%和32%。 貝伐珠單抗聯合含鉑雙藥化療成為驅動基因陰性的、晚期非鱗非小細胞肺癌標準的一線治療方案。 安羅替尼是一類口服、新型小分子多靶點酪氨酸激酶抑制劑(TKI)藥物,能夠有效抑制血管內皮生長因子受體(VEGFR)、血小板衍生生長因子受體(PDGFR)、成纖維細胞生長因子受體(FGFR)、c-Kit 等激酶,具有抗腫瘤血管生成和抑制腫瘤生長的作用。 2018年5月9日,中國生物制藥的附屬公司正大天晴藥業宣布:國家食品藥品監督管理總局(NMPA)已正式批準鹽酸安羅替尼用于晚期非小細胞肺癌(NSCLC)患者的三線治療。 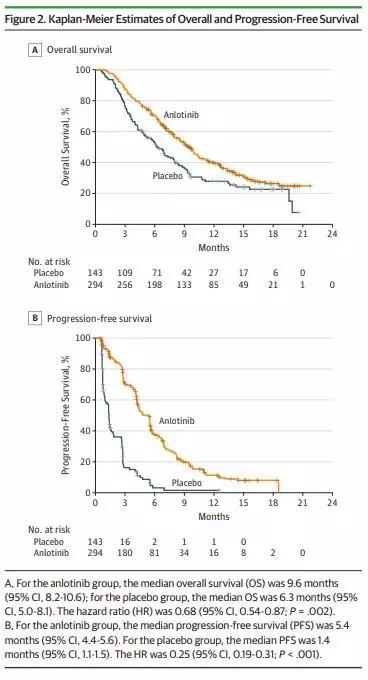 安羅替尼用于晚期NSCLC三線及以上治療的III期臨床研究ALTER0303,共納入了437例既往至少接受過兩次系統性化療方案治療的IIIB/IV期NSCLC患者,隨機接受安羅替尼(n=294)或安慰劑(n=143)治療,直至疾病進展或不可耐受的毒性。 結果顯示:安羅替尼單藥能夠顯著延長中位OS和PFS,OS延長3.3個月(9.6 vs 6.3個月; HR=0.68; 95%CI, 0.54-0.87; p=0.0018);PFS延長4.0個月(5.4 vs 1.4個月; HR=0.25; 95%CI, 0.19-0.31; p<0.0001)。 1997年,Folkman和O’Reilly等從小鼠內皮細胞瘤中分離到血管生成抑制因子—內皮抑素(Endostatin,ES),幾乎能完全抑制小鼠腫瘤誘導的血管生成,顯示較強的抗腫瘤活性,毒副作用輕。我國科學家羅永章等人開創性在Endostatin的N端外加了9個氨基酸,成功研發出了擁有自主知識產權的抗腫瘤血管靶向治療1類新藥:重組人血管內皮抑素注射液(恩度,Endostar)。 上市11年以來,恩度抗血管生成聯合化療已經成為中國晚期NSCLC一線治療的標準方案。對于晚期NSCLC特定人群,恩度同樣表現出優越的療效,包括:EGFR突變患者、伴惡性胸腔積液患者、腦轉移患者及老年患者。 2005年9月恩度被CFDA(原SFDA)批準聯合長春瑞濱/順鉑用于中國晚期非小細胞肺癌(NSCLC)患者的治療。目前恩度抗血管生成聯合化療已經成為中國晚期非小細胞肺癌一線治療的標準方案。 Ⅲ期臨床試驗: 2003年4月至2004年7月由中國工程院院士孫燕教授牽頭,中國醫學科學院腫瘤醫院聯合全國24家臨床醫院,對恩度進行了493例晚期非小細胞性肺癌(NSCLC)患者Ⅲ期臨床試驗。 結果顯示:安慰劑組和恩度組患者的有效率(RR)分別為19.5%和35.4%(P=0.0003),臨床獲益率(CBR)分別為64.0%和73.3%(P=0.035),中位腫瘤進展時間(TTP)分別為3.6個月和6.3個月(P<0.001),1年生存率分別為63.4%和74.3%(P=0.0000)。 上述3種肺癌血管生長成抑制劑藥物,均單獨或與化療藥物聯用獲批晚期非小細胞肺癌的治療,且相應的生存數據均優于單獨使用化療藥物,且據小編查詢,3種藥物均已經進入國家醫保藥物報銷名錄。
報銷標準:1998元(100mg(4ml)/瓶) 報銷范圍:限晚期轉移性結直腸癌或晚期非鱗非小細胞肺癌。
報銷標準:630元(15mg/2.4×10^5 U/3ml/支) 報銷范圍:限晚期非小細胞肺癌患者。
報銷標準:487元(12mg/粒);423.6元(10mg/粒);357元(8mg/粒) 報銷范圍:限既往至少接受過2種系統化療后出現進展或復發的局部晚期或轉移性非小細胞肺癌患者。 基因檢測報告顯示無對應靶向藥可用,免疫藥物獲益低且貴,那小編給你介紹的腫瘤抗血管生成抑制劑是一個不錯的選擇,當然因為每個患者的實際情況有所不同,因此是否能夠使用腫瘤抗血管生成抑制劑藥物,還需遵循臨床醫生的指導建議,不可私下用藥哦~ 湖南時代基因擁有一支以分子生物學、藥物基因組學、臨床醫學、計算機科學為主的復合型專業技術團隊,致力于腫瘤、心血管疾病等重大疾病的精準診斷和臨床個性化治療醫學檢驗服務、腫瘤液體活檢技術的臨床應用與科研服務、轉化醫學服務。 若各位小伙伴對肺癌基因檢測或相關藥物信息感興趣的話,歡迎致電400-700-2166,小編24小時為大家提供咨詢服務 參考文獻: https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?event=BasicSearch.process Hallmarks of cancer: the next generation. Cell. 2011 Mar 4;144(5):646-74. Shih Y C T, Smieliauskas, F, Geynisman, D. M, et al. Trends in the Cost and Use of Targeted Cancer Therapies for the Privately Insured Nonelderly: 2001 to 2011[J]. Journal of Clinical Oncology, 2015, 33(19):2190-2196. Effect of Anlotinib as a Third-Line or Further Treatment on Overall Survival of Patients With Advanced Non-Small Cell Lung Cancer The ALTER 0303 Phase 3 Randomized Clinical Trial. JAMA Oncology. 2018 Nov 1;4(11):1569-1575. Wang JW,Sun Y,Liu YY. Recombinant human endostatin combined with NP therapy advanced NSCLC randomized,double- blind,controlled,multi-center clinical study period Ⅲ[J].Chinese Journal Lung Cancer,2005,8(4):283-290. Wang J, Sun Y, Qin S. Results of phase IV clinical trial of combining endostar with chemotherapy for treatment of advanced non-small cell lung cancer (NSCLC)[J]. Journal of Clinical Oncology, 2010, 28(15)
|